2. 华南理工大学, 广州 510006
2. South China University of Technology, Guangzhou 510006
酚醛树脂作为最早实现工业化合成的树脂,虽已有百余年历史,但由于其耐热耐烧蚀性能优异、机械性能良好、成型加工性强、原料易得价格低廉,仍是一个理想的烧蚀防热用基体树脂[1]。酚醛树脂固化物中结构单元主要通过亚甲基桥交联形成三维网状结构,根据取代位置的不同可将亚甲基分为邻-邻位(o-o')、邻-对位(o-p)、对-对位(p-p')。酚醛树脂热解实验表明,热解过程包括亚甲基桥的断裂、氧化以及酚羟基之间环化脱水反应等,最终产生H2O、CO、CO2、苯酚及其衍生物、苯及其衍生物和稠环化合物等[2-9]。热解反应直接影响酚醛树脂基复合材料的烧蚀性能。以往的相关工作均通过实验方法研究酚醛树脂热解的化学结构变化规律,反应动力学分析以及残碳结构特征和应用。应用量子化学计算理论研究有机物的热解机理是一种有效的研究方法[10-11]。本文选取2BHM为模型化合物,并采用量子化学计算理论密度泛函理论(DFT)中的B3LYP/6-311G(d, p)方法,对2BHM的各种可能的热解反应路径进行了热力学与动力学计算分析,最后通过实验验证计算结果。
1 模拟与计算为深入了解酚醛树脂的热解机理,选取酚醛树脂的一个模型化合物邻位双羟苯基甲烷(2BHM)为研究对象,采用密度泛函理论(DFT)中的B3LYP/6-311G(d, p)方法,对2BHM热解反应路径进行了量子计算研究。
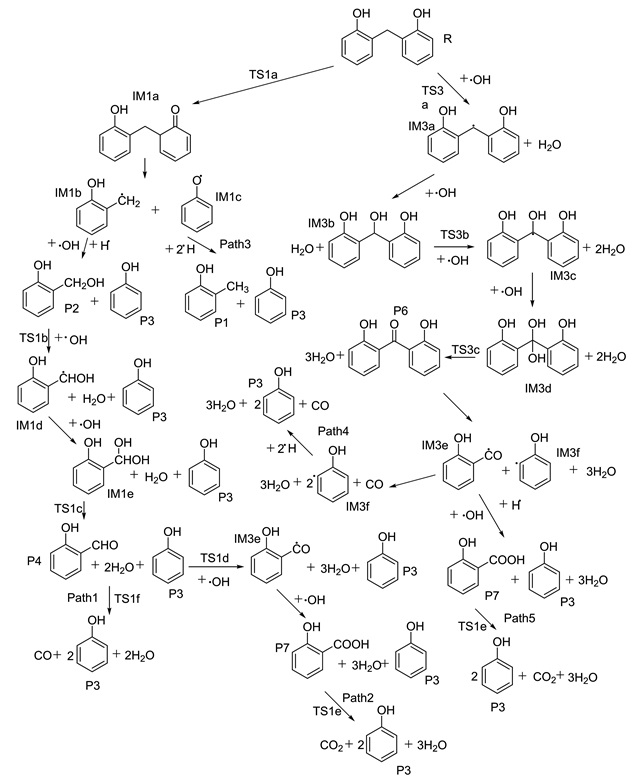
1.1 反应路径设计与计算方法根据文献[2-9]设计2BHM的六条热解反应路径如图 1所示。
|
| 图 1 模型化合物热解反应路径 Figure 1 Pyrolysis reaction paths of the model compound 2BHM |
采用Gaussian 09程序中密度泛函(DFT)理论B3LYP/6-311G(d, p)方法,对所有反应物、产物、中间体及过渡态进行了几何构型全优化和频率计算,并对热力学量考虑了振动零点能(ZPE)校正。用TS方法寻找各反应路径的过渡态,振动频率计算表明有唯一的虚频。最后用内反应坐标积分方法(IRC)跟踪反应路径来验证过渡态的正确性。计算700 ℃下热解反应的各种标准热力学参数。计算[12]各反应的标准热力学量变值等于经零点能校正后的产物的热力学量与反应物的热力学量的差值;反应活化能(反应能垒)等于绝对零度时过渡态的总能量与反应物的总能量之差。而对于自由基耦合反应(也即自由基终止反应),反应速率非常大,活化能极小(通常为10 kJ/mol左右,甚至更低),可认为不存在能垒;对于均裂产生自由基的反应,其键解离能可作为活化能。键解离能计算公式为[13]:
| $ \begin{array}{l} {D_0}\left( {R - X} \right) &=& E\left( R \right) + {E_{{\rm{ZPE}}}}\left( R \right) + E\left( X \right) + \\ &&{E_{{\rm{ZPE}}}}\left( X \right) - E\left( {RX} \right) - {\rm{ }}{E_{{\rm{ZPE}}}}\left( {RX} \right) \end{array} $ |
式中,D0为考虑零点修正时的键离解能,E为分子能量,EZPE为零点能校正能量。
1.2 反应物、产物、中间体和过渡态的几何优化表 1列出反应物,部分产物、中间体、过渡态经Gaussian 09中B3LYP/6-311G(d, p)方法计算得到优化后的部分键长、键角以及二面角等几何参数。根据对反应物、产物、中间体以及过渡态振动频率分析,所得反应物、产物和中间体均无虚频存在,所得过渡态有且仅有一个虚频,且虚频振动方向为反应方向。因此,经计算优化得到的所有分子结构是可靠的。
| species | structure parameter | |||
| bond length(0.1 nm) | bond angle/(°) | dihedral angle/(°) | ||
| R |  |
R(1, 11) 1.522 | A(1, 11, 12) 107.8877 | D(6, 3, 2, 1) -0.3482 |
| R(2, 8) 1.0858 | A(2, 3, 6) 119.0831 | D(8, 2, 1, 11) -0.0053 | ||
| R(4, 14) 1.3614 | A(2, 3, 7) 120.2473 | D(2, 1, 11, 12) -21.718 | ||
| R(11, 13) 1.0932 | A(4, 14, 15) 112.1796 | D(2, 3, 11, 16) 98.7597 | ||
| R(14, 15) 0.9696 | A(16, 17, 26) 117.019 | D(12, 11, 16, 18) 39.0113 | ||
| TS1a | 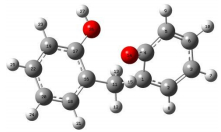 |
R(1, 11) 1.5674 | A(1, 4, 14) 108.3725 | D(6, 3, 2, 1) -2.8618 |
| R(2, 3) 1.372 | A(2, 3, 6) 120.4013 | D(6, 3, 2, 8) 171.6626 | ||
| R(3, 7) 1.0834 | A(2, 3, 7) 120.5984 | D(3, 2, 1, 4) -11.0684 | ||
| R(4, 14) 1.288 | A(2, 1, 11) 113.5135 | D(3, 2, 1, 11) 130.6649 | ||
| R(11, 13) 1.0941 | A(4, 14, 15) 75.522 | D(14, 4, 5, 9) -23.7376 | ||
| IM1a | 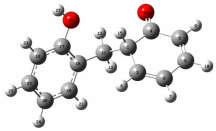 |
R(1, 2) 1.4988 | A(2, 1, 4) 115.1494 | D(4, 1, 2, 3) 8.1584 |
| R(1, 11) 1.5561 | A(2, 1, 15) 106.707 | D(11, 1, 2, 3) 137.2304 | ||
| R(1, 15) 1.1021 | A(1, 2, 3) 122.4526 | D(11, 1, 2, 8) -44.4056 | ||
| R(3, 7) 1.0842 | A(1, 11, 13) 106.19 | D(15, 1, 2, 3) -106.4769 | ||
| R(4, 14) 1.2197 | A(1, 11, 16) 114.4562 | D(15, 1, 2, 8) 71.8871 | ||
| P4 | 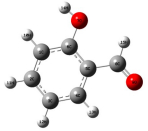 |
R(1, 2)1.39 | A(2, 1, 6)120.011 | D(6, 1, 2, 3)0.0 |
| R(1, 6)1.398 | A(6, 1, 10)119.685 | D(6, 1, 2, 11)180.0 | ||
| R(1, 10)1.086 | A(1, 2, 11)119.239 | D(10, 1, 2, 11)0.0 | ||
| R(3, 4)1.386 | A(4, 3, 12)120.516 | D(10, 1, 6, 7)0.0 | ||
| R(3, 12)1.083 | A(5, 4, 13)117.186 | D(1, 2, 3, 4)0.0 | ||
| P7 | 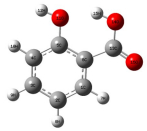 |
R(1, 2)1.388 | A(2, 1, 6)121.793 | D(6, 1, 2, 3)0.001 |
| R(1, 6)1.4 | A(6, 1, 7)116.843 | D(7, 1, 2, 3)180.001 | ||
| R(1, 7)1.083 | A(4, 5, 11)120.686 | D(7, 1, 2, 8)0.0 | ||
| R(5, 6)1.405 | A(1, 6, 5)117.774 | D(2, 1, 6, 5)-0.001 | ||
| R(11, 12)0.963 | A(5, 6, 13)125.707 | D(1, 2, 3, 9)-180.0 | ||
| TS3a | 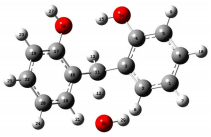 |
R(1, 2) 1.3892 | A(2, 1, 6) 119.3766 | D(6, 1, 2, 3) -0.1861 |
| R(1, 7) 1.0836 | A(6, 1, 7) 120.4929 | D(6, 1, 2, 8) 177.957 | ||
| R(3, 11) 1.5122 | A(3, 4, 14) 123.0571 | D(2, 3, 11, 12) -33.0386 | ||
| R(4, 14) 1.3617 | A(5, 4, 14) 116.8146 | D(2, 3, 11, 13) -147.7105 | ||
| R(14, 15) 0.9706 | A(3, 11, 12) 108.0137 | D(4, 3, 11, 12) 145.5475 | ||
| IM3a | 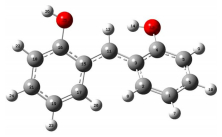 |
R(1, 2) 1.385 | A(2, 1, 6) 119.9627 | D(6, 1, 2, 3) 0.0152 |
| R(1, 7) 1.0838 | A(2, 1, 7) 119.8317 | D(7, 1, 2, 3) 178.6958 | ||
| R(3, 11) 1.4377 | A(2, 3, 11) 124.0867 | D(7, 1, 6, 5) -178.9085 | ||
| R(4, 13) 1.364 | A(5, 4, 13) 117.0568 | D(1, 2, 3, 11) -175.3597 | ||
| R(13, 14) 0.9643 | A(3, 11, 15) 128.7954 | D(2, 3, 11, 12) 148.1733 | ||
| P6 | 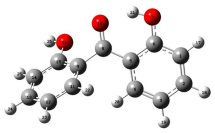 |
R(1, 2) 1.3836 | A(2, 1, 6) 120.2621 | D(6, 1, 2, 3) 0.0768 |
| R(1, 17) 1.0831 | A(6, 1, 17) 118.0067 | D(17, 1, 2, 3) -179.2098 | ||
| R(6, 7) 1.3372 | A(4, 5, 8) 122.3502 | D(4, 5, 8, 10) -173.583 | ||
| R(7, 21) 0.9883 | A(6, 7, 21) 106.6439 | D(5, 8, 9, 15) -121.4542 | ||
| R(8, 10) 1.2342 | A(8, 9, 15) 120.4259 | D(10, 8, 9, 15) 59.9654 | ||
在优化了平衡几何构型的基础上,对所有中间体以及过渡态做热力学ZPE校正,得到校正后的总能量,经过整理得到不同路径各个基元反应的活化能,不同路径的势能剖面如图 2和图 3所示。
|
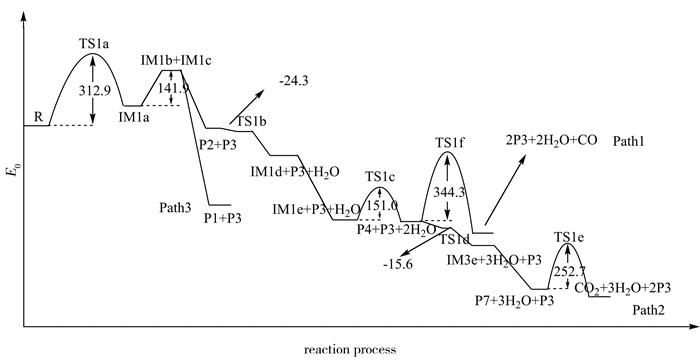
| 图 2 路径1~3的势能剖面图 Figure 2 Potential energy profiles along reaction pathways 1-3 |
|
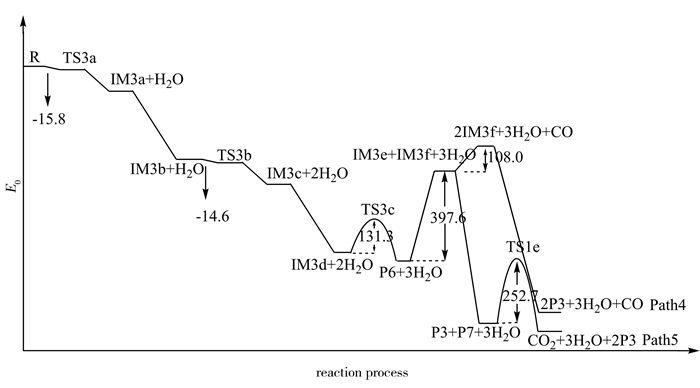
| 图 3 路径4和路径5的势能剖面图 Figure 3 Potential energy profiles along pathway 4 and 5 |
图 2为反应路径1-3的势能剖面图。反应物2BHM首先分子异构形成醌酮结构,异构活化能为312.9 kJ/mol,活化能比较高,但是比反应物直接断亚甲基能垒要低(直接断键活化能为351.1 kJ/mol)。而后断裂生成甲酚自由基(IM1b)和酚氧自由基(IM1c),能垒为141.9 kJ/mol。IM1b与羟基自由基发生耦合反应生成水杨醇(P2),放出大量热。水杨醇羟甲基中C原子上的H被羟基自由基夺去生成水和中间体IM1d,此步骤经计算得到能垒为负值,但是所得过渡态有且仅有一个虚频,且虚频振动方向为反应方向。这在Gaussian应用中是一个比较常见的问题,出现这种情况的原因有二:其一,由于计算方法的不精确,导致算得的能垒为负值;其二,有可能水杨醇和羟基自由基形成反应复合物[14-15]。无论以上何种情况,可以确定的是这个反应的能垒非常低。IM1d继续和OH自由基耦合形成双羟基化合物IM1e,双羟基不稳定发生分子内脱水形成水杨醛(P4),此反应活化能为151.0 kJ/mol。水杨醛的热解存在两种方式,即路径1和2。路径1,直接脱羰基热解产生CO和苯酚,活化能为344.3 kJ/mol;路径2,与路径1中羰基直接热解不同,羰基被OH自由基氧化成水杨酸(P7),并最终脱羧产生CO2和苯酚,反应第一步无能垒,反应第二步脱羧是反应控制步骤,能垒为252.7 kJ/mol。对比反应路径1和2,可知路径1直接脱羰基热解需要克服比较高的能垒,反应不易发生,而路径2中水杨酸脱羧基活化能要低于路径1中羰基断裂活化能,因此水杨醛更倾向于形成水杨酸后脱羧,路径2是水杨醛的主要热解路径,热解更倾向于产生CO2。路径3,形成的中间体IM1b和IM1c直接结合H原子终止反应产生邻-甲苯酚(P1)和苯酚,此过程无能垒。对比路径1~3,从图 2可看出形成邻-甲苯酚和苯酚所释放的能量高于生成水杨醇和苯酚,根据能量最低原理,可知自由基IM1b更倾向于结合羟基自由基生成邻甲酚,这表明路径3占优。
由图 3路径4和5的势能剖面图可知,反应物被羟基自由基最终氧化成苯甲酮(P6),苯甲酮均裂产生自由基IM3e和IM3f。计算反应第一步生成IM3a和第三步生成IM3c的能垒,算得的结果为负值(前者为-15.8 kJ/mol,后者为-14.6 kJ/mol),与前面讨论的情况一样,表明这两步活化能很低。反应第二步和第四步为自由基耦合反应,无能垒。第四步形成的双羟基化合物IM3d,不稳定脱水生成苯甲酮,反应活化能较低为131.3 kJ/mol。苯甲酮均裂产生IM3e和IM3f的反应活化能为397.6 kJ/mol,反应能垒较高。后续热解有两个途径,分别为Path5和Path6,前者终产物为CO、苯酚和H2O,后者终产物为CO2、苯酚和H2O。路径4,IM3e中羰基断键生成CO和IM3f,活化能为108.0 kJ/mol,IM3f与氢原子耦合产生苯酚,放出大量的热。途径6,与路径2后半段一样,IM3e与OH自由基耦合成水杨酸,无能垒,水杨酸脱羧产生CO2和苯酚,能垒为252.7 kJ/mol。与前面讨论情况类似,由于路径5中生成P3和P7是自由基终止反应,无活化能,而路径4在生成CO和IM3f这一步反应步骤中,活化能为108.0 kJ/mol,因此可知,路径5更容易进行,故热解更倾向于生成CO2。
经过以上动力学分析,路径1的反应控速步骤为水杨醛P4脱醛基生成CO,反应活化能为344.3 kJ/mol;路径2和3的控速步骤反应物R醌酮化,活化能为312.9 kJ/mol;路径4和路径5的控速步骤为苯甲酮P6断键生成自由基IM3e和IM3f,反应活化能为397.6 kJ/mol,由上可知路径2和3的控速步骤活化能最低,路径1次之,路径4和5最高。此外,经过前面的分析我们知道路径3要优于路径1和2,而路径5要优于路径4。
综上所述,反应物2BHM的热解路径优先顺序依次为Path 3>Path 2>Path 1>Path 5>Path 4,相对应的苯酚和邻甲酚是2BHM最主要的热解产物,另外,所有路径的终产物中均有苯酚,因此热解产物中苯酚更占主要。根据路径2优先于路径1以及路径5优先于路径4可知,生成CO2的反应要比生成CO的反应容易进行,据此推测2BHM的热解产物中就CO2和CO而言,前者的含量应该会明显高于后者。
2 实验验证以一种中国科学院化学研究所提供的线性酚醛树脂为原料,将其置于在700 ℃下进行热解实验,根据实验结果以验证前面计算结果的准确性。
傅里叶红外分析(FT-IR):采用美国Perkin Elmer公司的Spotlight 400型傅里叶变换红外光谱仪配备金刚石池单次衰减全反射(Attenuated Total Reflection, ATR)红外光谱法测试。扫描范围550~4 000 cm-1,扫描速率为0.2 cm-1/s,采集分辨率为4/cm,扫描8次。
裂解气相色谱质谱联用分析(PyGC-MS):取一定量的酚醛树脂固化物粉末(2 mg),置于日本Frontier系列PY.2020S管式炉裂解器中,在指定温度下进行裂解实验。以氦气为载气,所得裂解气采用日本岛津GCMS.QP2010 Ultra热解气相色谱-质谱联用仪进行解析。分离所用色谱柱为30 m长的石英毛细管。分离时色谱柱于40 ℃恒温3 min后,以10 ℃/min的速率升温至260 ℃,并在260 ℃恒温10 min。质谱检测EI离子源为0.80 kV,接口温度为260 ℃,进样口温度为260 ℃。
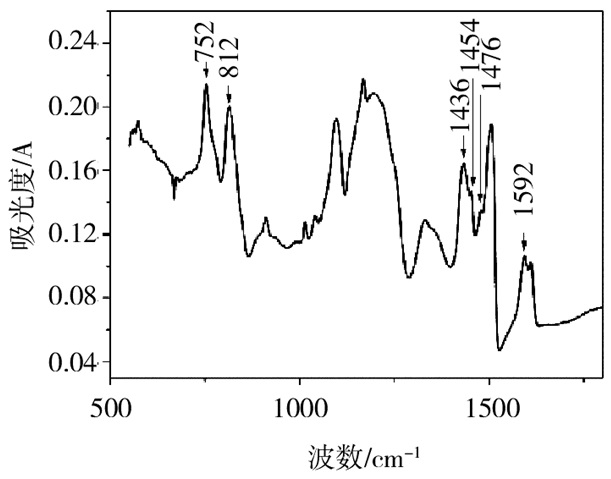
3 结果与讨论图 4给出了线性酚醛树脂在500~1 800 cm-1的红外谱图,酚羟基的吸收峰3 300 cm-1此处并未列出,可看出此线性酚醛树脂主要包含结构为苯环(1 592 cm-1)和亚甲基,邻邻位亚甲基(o-o', 1 436 cm-1)具有很强的吸收峰,而邻对位亚甲基(o-p, 1 454 cm-1)和对对亚甲基(p-p', 1454 cm-1)吸收峰较弱,这表明此线性酚醛树脂中苯环之间主要通过邻邻位亚甲基相连,而邻对位亚甲基和对对亚甲基较少,752 cm-1处苯环邻位取代结构的特征吸收峰明显高于812 cm-1处苯环对位取代结构的特征吸收峰也说明了这一点。
|
| 图 4 线性酚醛树脂的红外谱图 Figure 4 FT-IR spectrum of novolac resin |
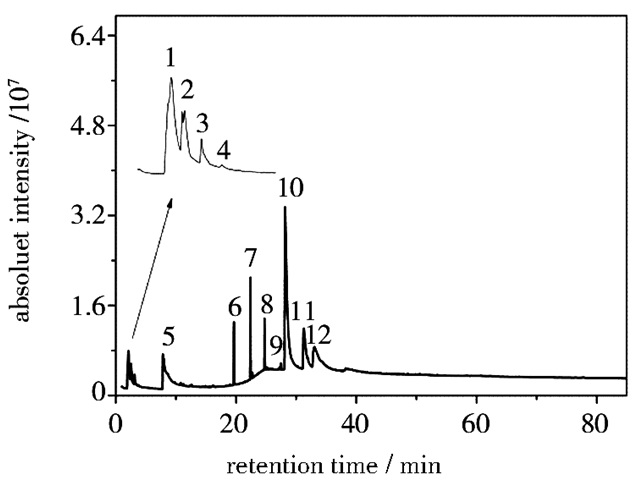
将线性酚醛树脂置于700 ℃下进行热裂解测试,并对其裂解产物进行归一化法半定量分析,裂解产物色谱图如图 5所示,表 2是其主要产物相应的质谱鉴定结果以及半定量结果。
|
| 图 5 700 ℃下线性酚醛树脂裂解气相色谱图 Figure 5 The PyGC of novolac resin at 700 ℃ |
| 序号 | 产物 | 相对分子质量 | 含量/% |
| 1 | CH4 | 16 | 6.78 |
| 2、3 | CO2 | 44 | 4.41 |
| 4 | 乙烷 | 30 | 0.05 |
| 5 | H2O | 18 | 12.60 |
| 6 | 苯 | 78 | 2.59 |
| 7 | 甲苯 | 92 | 4.21 |
| 8 | 间二甲苯 | 106 | 2.11 |
| 9 | 1, 3, 5-三甲苯 | 120 | 0.17 |
| 10 | 苯酚 | 94 | 43.29 |
| 11 | 邻甲酚 | 108 | 11.95 |
| 12 | 对甲酚 | 108 | 11.85 |
由表 2可看出700 ℃时线性酚醛树脂热解产物主要包括水、苯酚、邻甲酚和对甲酚,除此之外有少量甲烷、CO2、苯、甲苯和间二甲苯以及痕量乙烷和1, 3, 5-三甲苯。水由苯环上羟基脱除后结合氢原子产生,产物中包含苯及其甲基取代物说明了这一点。苯酚及其甲基取代物由亚甲基桥断裂产生,此类产物含量极高,表明树脂此时反应主要以亚甲基断键为主,其中苯酚的含量最高,对甲酚含量最低,这也与线型酚醛树脂苯环之间主要以邻邻位相连是一致的。少量的CO2由亚甲基断裂后结合羟基自由基形成醇而后被氧化成醛后最终被羟基自由基氧化成羧基并脱羧产生或者亚甲基被羟基自由基氧化成羰基后断键形成,反应中的羟基自由基具有极强的氧化性,可以由酚羟基脱除以及水高温分解得到。甲烷和乙烷是由亚甲基断裂时结合氢原子或相互结合产生。
线性酚醛树脂700 ℃下裂解产物中,苯酚的含量为最高,水次之,其次是邻甲酚,这与前面的计算结果是一致的。另外产物中存在CO2而并没有CO,可能是含量太少而仪器并未检测出来或者是反应不产生CO,无论哪种情况均说明醛基和羰基更倾向于形成羧基后最终脱羧生成CO2而非直接断键生成CO,这与前面计算结果也是一致的。
4 结论(1) 根据计算结果,酚醛树脂的一种模型化合物2BHM的最优热解路径为Path3,相应的主要热解产物为苯酚和邻甲酚,由于所有路径的终产物中均有苯酚,因此热解产物中苯酚为主要成分。生成CO2的反应要比生成CO的反应容易进行。
(2) 与模型化合物2BHM结构类似的一种线性酚醛树脂热解产物中苯酚含量最高,而且热解产物中并未出现CO。以上说明计算结果与实验结果是基本一致的,表明应用量子化学计算理论研究酚醛树脂的热解机理是一种有效的研究方法,可以利用该理论方法深入研究酚醛树脂的热解机理。
| [1] |
郑顺兴. 烧蚀材料与耐烧蚀酚醛树脂[J].
南京航空航天大学学报, 1996, 28(2): 253–258.
|
| Cited By in Cnki (25) | |
| [2] | FITZER E, SCHAFER W. The effect of crosslinking on the formation of glasslike carbons from thermosetting resins[J]. Carbon, 1970, 8(3): 353–364. |
| Click to display the text | |
| [3] | JACKSON W M, CONLEY R T. High temperature oxidative degradation of phenol-formaldehyde polycondensates[J]. Journal of Applied Polymer Science, 1964, 8(5): 2163–2193. |
| Click to display the text | |
| [4] | OUCHI K. Infra-red study of structural changes during the pyrolysis of a phenol-formaldehyde resin[J]. Carbon, 1966, 4(1): 59–66. |
| Click to display the text | |
| [5] | TRICK K A, SALIBA T E. Mechanisms of the pyrolysis of phenolic resin in a carbon/phenolic composite[J]. Carbon, 1995, 33(11): 1509–1515. |
| Click to display the text | |
| [6] | BENNETT A, PAYNE D R, COURT R W. Pyrolytic and elemental analysis of decomposition products from a phenolic resin[J]. Macromolecular Symposia, 2014, 339(1): 38–47. |
| Click to display the text | |
| [7] | WONG H W, PECK J, BONOMI R E, et al. Quantitative determination of species production from phenol-formaldehyde resin pyrolysis[J]. Polymer Degradation & Stability, 2015, 112: 122–131. |
| Click to display the text | |
| [8] |
张西莹, 刘育红. 酚醛树脂/碳化硼/聚硼氮烷复合物的固化行为及其热解性能[J].
化工学报, 2014, 65(8): 3268–3276.
|
| Cited By in Cnki (3) | |
| [9] |
徐复铭, 周伟良. Resol型酚醛树脂热解特征的TG-MS研究[J].
宇航材料工艺, 2003, 33(1): 18–23.
|
| Cited By in Cnki (25) | |
| [10] |
吴永标, 刘德飞, 吴颖, 等. MOF-5上甲醇、乙醛和丙酮吸附机理的密度泛函理论研究[J].
化工学报, 2013, 64(8): 2891–2897.
|
| Cited By in Cnki (3) | |
| [11] |
王甫洋, 陈建挺, 朱维廷, 等. 多氯代二苯并噻吩亚砜热力学性质的密度泛函理论研究[J].
化工学报, 2010, 61(1): 1–9.
|
| Cited By in Cnki (1) | |
| [12] |
贾建波, 曾凡桂, 李美芬, 等. 用密度泛函理论研究煤中甲基苯生成甲烷的反应机理[J].
化工学报, 2010, 61(12): 3235–3242.
|
| Cited By in Cnki (20) | |
| [13] |
张芳沛, 程新路, 刘子江, 等. 硝酸丙酯键离解能和热解机理的密度泛函理论研究[J].
高压物理学报, 2005, 19(2): 189–192.
|
| Cited By in Cnki (8) | |
| [14] | WU X N, ZHAO Y X, XUE W, et al. Active sites of stoichiometric cerium oxide cations (CemO2m+) probed by reactions with carbon monoxide and small hydrocarbon molecules.[J]. Physical Chemistry Chemical Physics Pccp, 2010, 12(16): 3984–3997. |
| Click to display the text | |
| [15] | ZHAO Y X, WU X N, MA J B, et al. Experimental and theoretical study of the reactions between vanadiumsilicon heteronuclear oxide cluster anions with n-butane[J]. Journal of Physical Chemistry C, 2010, 114(28): 12271–12279. |
| Click to display the text |


